Introduction du virus mpox dans les îles du Sud-Ouest de l’océan Indien
Ambroise Mercier1,2, Mélissa Bérot3, Sylvain Brisse4, Marie-Pierre Moiton5, Olivier Belmonte1, Laurent Souply1, Guillaume Miltgen1,2,6
- Laboratoire de Bactériologie, CHU Félix Guyon, Saint-Denis, La Réunion, France.
- UMR Processus Infectieux en Milieu Insulaire Tropical (PIMIT), CNRS 9192, INSERM U1187, IRD 249, Université de La Réunion, Saint-Denis, La Réunion, France.
- Département de la Sécurité et des Urgences Sanitaires, Agence Régionale de Santé de Mayotte, Mamoudzou, France.
- Unité Biodiversité et Epidémiologie des Bactéries Pathogènes, Institut Pasteur, Paris, France.
- Service de Maladies Infectieuses, CHU de La Réunion, Saint-Denis, La Réunion, France.
- Centre Régional en Antibiothérapie (CRAtb) de La Réunion, Saint-Pierre, France.
Mots-clés : Mpox ; épidémie ; clade Ib ; Océan Indien ; Réunion ; Mayotte.
Introduction
La mpox ou variole B, est une zoonose causée par le virus mpox (mpox virus [MPV], anciennement monkeypox virus). Ce virus appartient au genre Orthopoxvirus (famille des Poxviridae) qui comprend d’autres représentants tels que le virus de la variole (variola virus [VARV]), de la vaccine (vaccinia virus [VACV]) ou encore de la variole de la vache (cowpox virus [CPV]) (1). Cette zoonose, moins sévère que la variole, a pour hôtes les rongeurs (funisciures, cricétomes des savanes, loirs…) et les primates (dont l’humain) (2). Depuis l’éradication de la variole en 1977 grâce à la vaccination, le MPV et le CPV sont les Orthopoxvirus les plus étudiés du fait de leur fort potentiel épidémique (3).
Le MPV, initialement distribué en Afrique, a été responsable de nombreuses épidémies de mpox à travers le monde. Ce virus a été découvert pour la première fois dans une animalerie à Copenhague en 1958 chez des primates (4). Ce n’est qu’en 1970 qu’il a été décrit chez l’humain, en République démocratique du Congo (5). Dès lors, d’autres cas ont été signalés en Afrique. La première épidémie extra-Africaine a eu lieu en 2003 aux États-Unis où des chiens de prairie domestiques avaient été infectés au contact de cricétomes des savanes infectés provenant du Ghana (6). En 2022, une nouvelle épidémie mondiale est survenue et était caractérisée par une transmission interhumaine via des contacts directs avec les lésions cutanéo-muqueuses des patients infectés, essentiellement des hommes ayant des rapports sexuels avec des hommes (HSH) (7).
Phylogénétiquement, le MPV est divisé en deux clades sur la base des séquences génomiques, le clade I d’Afrique centrale présentant une sévérité et une mortalité plus élevées que le clade II d’Afrique de l’Ouest (8). Les caractéristiques épidémio-cliniques des différents clades sont résumées dans le Tableau 1 (9).
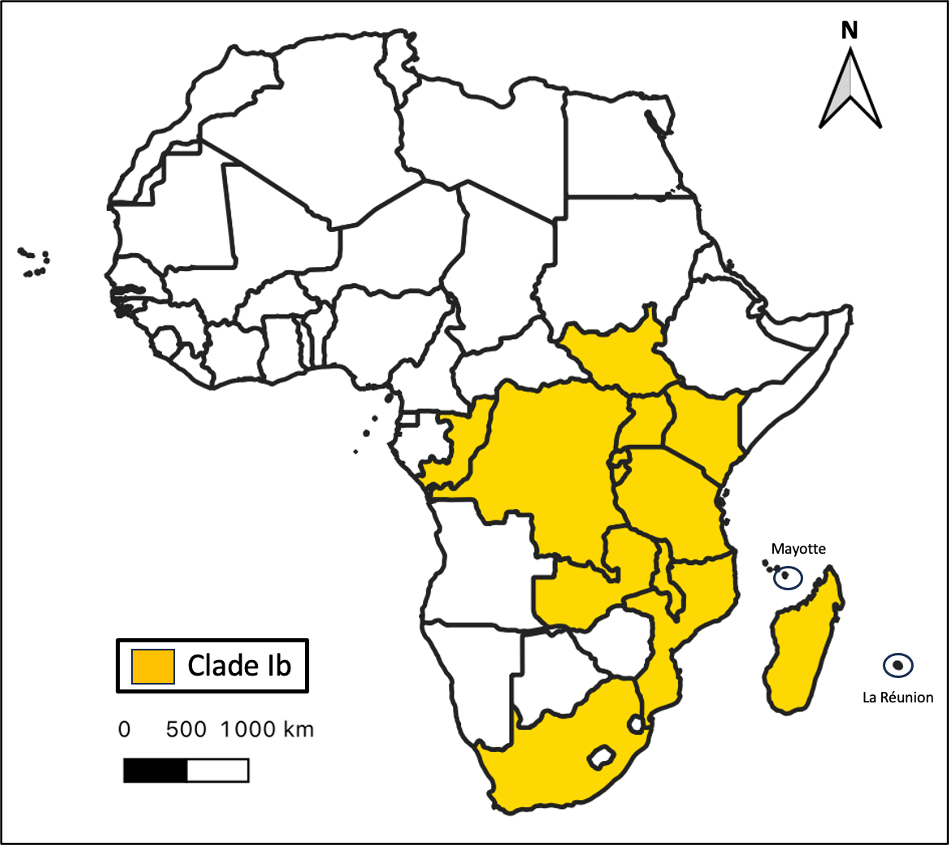
L’épidémie causée par le MPV de clade Ib a émergé en 2023 en République démocratique du Congo et dans les pays alentours (10). En 2024-2025, des cas ont été déclarés en dehors de l’Afrique, comme aux USA (11) ainsi qu’en Europe avec des cas observés chez des voyageurs en retour de zone d’endémie (12) mais aussi autochtones (13) ou nosocomiaux (14). Des cas d’infection par un MPV de clade Ib ont été signalés à partir de décembre 2025 dans les territoires du Sud-Ouest de l’océan Indien, en provenance la région côtière de Mahajanga à Madagascar, où plus de deux-cents cas ont été confirmés (Figure 1, 15). D’autres cas de mpox ont également été déclarés en dehors de Madagascar, notamment aux Comores où 16 cas ont été confirmés essentiellement à Grande Comore (données au 19/02/2026, 16).
Tableau 1. Épidémiologie des clades du virus mpox (adapté de Beiras et al., 2025, 9)
| Clade | Période | Distribution | Transmission | Épidémies | Population |
| Ia | 1970-2024 | Afrique centrale | Zoonotique | Incidence faible | Enfants |
| Ib | 2023 | RDC | Interhumaine | Émergence en 2023 | Adultes et enfants |
| IIa | 1970-2018 | Afrique de l’Ouest | Zoonotique | Endémie aux USA en 2003 | Adultes et enfants |
| IIb lignée A | 2017-2024 | Nigeria | Zoonotique + interhumaine | Épidémie Nigéria 2017 | Adultes |
| IIb lignée B | 2022-2023 | Distribution mondiale | Sexuelle | Épidémie mondiale 2022 | HSH* |
* Hommes ayant des rapports sexuels avec des hommes.
Le 8 janvier 2026, un premier cas a été diagnostiqué à Mayotte. Neuf autres cas supplémentaires ont été confirmés depuis (15). Le 22 janvier 2026, le premier cas de mpox causé par le clade Ib a été confirmé à La Réunion (17). Ce patient, résidant à La Réunion, a été adressé au CHU de La Réunion par son médecin traitant après un séjour à Madagascar. Cette introduction du MPV dans les territoires de l’océan Indien a fait l’objet d’un Message d’Information de Santé Publique (MISP) de la DGS le 5 février 2026 décrivant une situation épidémiologique très évolutive à Madagascar et susceptible de générer des cas d’importation sur l’ensemble du territoire national (18).
Cas documentés à Mayotte et à La Réunion
À Mayotte
Entre le 8 janvier et le 12 février 2026, dix cas confirmés de mpox ont été identifiés à Mayotte. Le clade Ib a été confirmé chez les premiers cas par le Centre National de Référence (CNR) des Orthopoxvirus (Institut de Recherche Biomédicale des Armées, Brétigny-sur-Orge). Tous les cas concernaient des adultes et une notion de contact sexuel a été rapportée pour l’ensemble des cas. Les individus présentaient des éruptions cutanées ou cutanéo-muqueuses polymorphes. Aucun cas grave n’a été observé.
Parmi les premiers cas, trois étaient liés à des séjours récents à Madagascar et ont été classés comme importés. Ces introductions ont donné lieu à quatre transmissions secondaires, notamment sexuelles et/ou par contacts intrafamiliaux. De plus, une chaîne de transmission a été identifiée à partir d’un cas secondaire attestant d’une transmission tertiaire locale. Un cas autochtone, sans lien épidémiologique formellement confirmé, a également été identifié.
Des investigations ont été menées autour de chaque cas afin d’identifier les contacts à risque et de mettre en œuvre les mesures de contrôle, incluant l’isolement et la vaccination post-exposition qui a concerné treize personnes. Une campagne de vaccination préventive ciblée en rapport avec les recommandations du Haut Conseil de Santé Publique (HCSP) a également été déployée sur le territoire.
À La Réunion
Quatre cas de mpox ont été identifiés à La Réunion au 20 février 2026. Le premier cas concernait un individu de retour d’un voyage de Madagascar où celui-ci avait déclaré un rapport sexuel non protégé. Le diagnostic a été confirmé après l’apparition de lésions génitales faisant suspecter une syphilis primaire ou une infection par MPV. L’évolution clinique a été favorable avec un traitement symptomatique et sous surveillance dermatologique (télé-consultation). Le second cas concernait également un patient revenant de Madagascar, présentant des lésions cutanées périnéales compatibles avec une infection par MPV. Ce second cas a généré 2 cas contacts secondaires. Aucune complication n’a été observée chez ces quatre patients. L’ensemble des bilans complémentaires à la recherche d’infections sexuellement transmissibles (IST) se sont révélés négatifs. Les quatre cas d’infections ont été confirmés comme liés au MPV de clade Ib par le laboratoire du Microbiologie du CHU de La Réunion.
Ces cas ont conduit à la mise en œuvre des mesures habituelles de contrôle, incluant l’isolement du cas index et la prophylaxie secondaire des contacts.
Au laboratoire
La prise en charge des prélèvements à visée diagnostique virologique pour la recherche du MPV est décrite dans la procédure opérationnelle de prélèvement de la Coordination Opérationnelle Risque Épidémique et Biologique (COREB) (19).
Les patients suspects présentant des signes cliniques évocateurs d’une infection à MPV avec exposition à risque (retour d’un voyage en zone d’endémie, partenaires sexuels multiples, HSH) sont systématiquement prélevés. Il est recommandé de réaliser un écouvillonnage et/ou prélèvement de biopsies des lésions cutanées au niveau des muqueuses (20). Pour les cas probables, le prélèvement est non systématique mais une fiche de déclaration obligatoire (DO) doit être communiquée à l’ARS.
Le MPV est un agent biologique de classe 3 (inscrit à la liste des Micro-Organismes et Toxines ou MOT, 21), nécessitant une décontamination des prélèvements ainsi qu’un transport en triple emballage (substance biologique de catégorie B, norme UN3373, instruction d’emballage P650) (20). Le diagnostic virologique se fait par des tests d’amplification des acides nucléiques (ou TAAN) reposant sur une PCR de genre Orthopoxvirus puis confirmation par PCR spécifique MPV ou directement par PCR spécifique MPV. Si positif, un typage (détermination du clade) par PCR est réalisé afin de discriminer le clade responsable des lésions (Ia, Ib, ou II), en ciblant des séquences spécifiques des gènes viraux G2R, C3L et C1B (22).
Le risque de contamination à partir des prélèvements biologiques varie selon le type de prélèvement ainsi que les conditions de transport et d’analyse. Il existe un risque significatif de contamination à partir des prélèvements biologiques pour les prélèvements cutanéomuqueux et ORL, alors que le risque est considéré comme faible pour les prélèvements sanguins et urinaires permettant une prise en charge standard de ces prélèvements.
Stratégies de contrôle, traitement et prévention
En France, la stratégie de réponse mpox repose sur la prévention (vaccination), la détection et confirmation par biologie moléculaire des cas (TAAN et séquençage), le signalement et prise en charge du cas index et des contacts (18).
Les éruptions vésiculeuses pouvant faire suspecter une infection par MPV doivent faire suggérer d’autres diagnostics différentiels tels que le syndrome pied-main-bouche (Enterovirus), la varicelle, l’herpès, la syphilis secondaire mais également d’autres dermatoses bulleuses non-infectieuses (24). De plus, il convient de réaliser un bilan IST systématique chez les patients ayant des rapports sexuels non protégés (sérologies HIV, HBV, HCV, syphilis et PCR Neisseria gonorrhoeae et Chlamydia trachomatis sur 1er jet urinaire) (25).
Le traitement des patients repose sur une prise en charge symptomatique (antalgiques de paliers 1 à 3) et, selon avis infectieux, un traitement spécifique peut être envisagé (técovirimat, brincidofovir, cidofovir, immunoglobulines) en fonction des comorbidités du patient (26).
Une prophylaxie vaccinale contre le MPV existe et consiste en un vaccin « antivariolique » de 3e génération (8). La vaccination contre la mpox est indiquée en pré-exposition chez les HSH et les individus transgenres ayant des partenaires sexuels multiples, les travailleuses du sexe, les professionnels des lieux de consommation sexuelle et les personnes partageant le même lieu de vie que des individus à risque. Le vaccin a démontré une bonne efficacité chez l’enfant pouvant développer des formes graves (27). Une vaccination post-exposition est également recommandée autour des cas (26). De plus, le HCSP recommande une vaccination pour les voyageurs en zone endémique (dont Madagascar) à savoir les personnels soignants, les travailleurs humanitaires à risque d’exposition, les personnes originaires de zones de circulation active, les expatriés (selon conditions de vie sur place) (28). Pour les femmes enceintes, les enfants et les patients immunodéprimés, le report du voyage doit être conseillé, ou si le voyage est maintenu, la vaccination des individus immunodéprimés doit être proposée, mais en l’état actuel des connaissances, ne l’est pas chez la femme enceinte et l’enfant. Du fait d’une efficacité incomplète de la vaccination, les autres mesures de prévention reposent sur l’hygiène des mains, l’isolement des cas, la limitation des contacts avec des individus susceptibles d’être infectés par le MPV et l’absence de partage de literie, objets ou linge de ces individus (18).
Conclusions et perspectives
De nombreux cas de mpox liés au MPV de clade Ib ont été confirmés récemment dans la région Sud-Ouest de l’Océan Indien nécessitant une vigilance clinique et une surveillance accrue. Cette situation épidémiologique est en évolution constante ; à ce jour (20/02/2026), dix cas ont été confirmés à Mayotte, quatre à La Réunion. Les infections par MPV sont des maladies à déclaration obligatoire qui doivent être déclarées sans délai aux Agences Régionales de Santé (ARS), sans attendre le typage (23).
L’extension de l’épidémie de mpox à ces îles satellites du continent Africain situées dans le Sud-Ouest de l’océan Indien souligne l’interconnexion de ces territoires, liée aux flux de population permis notamment par le trafic aérien. Il est fondamental de pouvoir organiser une réponse coordonnée dans la zone en rapport avec les autorités de santé locales à la fois régionales (ARS), nationales (DGS/Ministère) et internationales (OMS/COI ou Commission de l’océan Indien). L’évolution épidémiologique régionale, combinée au potentiel épidémique de ce virus, doivent faire prendre en compte cette progression de l’épidémie, afin de prévenir sa potentielle extension au territoire hexagonal.
Bibliographie
-
Alakunle E, Kolawole D, Diaz-Cánova D, Alele F, Adegboye O, Moens U, et al. A comprehensive review of monkeypox virus and mpox characteristics. Front Cell Infect Microbiol. 2024;14:1360586.
-
Doty JB, Malekani JM, Kalemba LN, Stanley WT, Monroe BP, Nakazawa YU, et al. Assessing Monkeypox Virus Prevalence in Small Mammals at the Human-Animal Interface in the Democratic Republic of the Congo. Viruses. 2017;9(10):283.
-
Yahya G, Mohamed NH, Wadan AHS, Castro EM, Kamel A, Abdelmoaty AA, et al. The Emerging Threat of Monkeypox: An Updated Overview. Viruses. 2026;18(1):69.
-
Parker S, Buller RM. A review of experimental and natural infections of animals with monkeypox virus between 1958 and 2012. Future Virol. 2013;8(2):129–57.
-
Bunge EM, Hoet B, Chen L, Lienert F, Weidenthaler H, Baer LR, et al. The changing epidemiology of human monkeypox-A potential threat? A systematic review. PLoS Negl Trop Dis. 2022;16(2):e0010141.
-
Reed KD, Melski JW, Graham MB, Regnery RL, Sotir MJ, Wegner MV, et al. The detection of monkeypox in humans in the Western Hemisphere. N Engl J Med. 2004;350(4):342–50.
-
Suñer C, Ubals M, Tarín-Vicente EJ, Mendoza A, Alemany A, Hernández-Rodríguez Á, et al. Viral dynamics in patients with monkeypox infection: a prospective cohort study in Spain. Lancet Infect Dis. 2023;23(4):445–53.
-
Elsayed S, Bondy L, Hanage WP. Monkeypox Virus Infections in Humans. Clin Microbiol Rev. 2022;35(4):e0009222.
-
Beiras CG, Malembi E, Escrig-Sarreta R, Ahuka S, Mbala P, Mavoko HM, et al. Concurrent outbreaks of mpox in Africa—an update. The Lancet. 2025;405(10472):86–96.
-
Satheshkumar PS, Gigante CM, Mbala-Kingebeni P, Nakazawa Y, Anderson M, Balinandi S, et al. Emergence of Clade Ib Monkeypox Virus—Current State of Evidence. Emerg Infect Dis. 2025;31(8):1516–25.
-
Tang EC, Haw M, Kulkarni S, Johnson E, Gigante CM, Balanji N, et al. Detection of Community Transmission of Clade Ib Mpox Virus in the United States. NEJM Evid. 2026;5(2):EVIDpha2500319.
-
Treutiger CJ, Filén F, Rehn M, Aarum J, Jacks A, Gisslén M, et al. First case of mpox with monkeypox virus clade Ib outside Africa in a returning traveller, Sweden, August 2024: public health measures. Euro Surveill. 2024;29(48):2400740.
-
Elsinga J, van de Ven C, de Vries A, Coppoolse H, Petrignani M, van Cleef B, et al. First detection and autochthonous transmission of monkeypox virus clade Ib in the Netherlands, October to November, 2025. Euro Surveill. 2026;31(3):2500958.
-
McLoughlin M, Fahey L, Carr M, Caceda B, Igoe D, Dean J, et al. Nosocomial transmission in a monkeypox virus clade Ib outbreak, Ireland, August to October 2025. Euro Surveill. 2025;30(50):2500926.
-
Global Mpox Trends [Internet]. World Health Organization. 2026. Available from: https://worldhealthorg.shinyapps.io/mpx_global/
-
Variole du singe aux Comores : 10 cas confirmés, six patients guéris et 63 cas contacts identifiés. Données du Ministère de la Santé, Union des Comores. Available from: https://la1ere.franceinfo.fr/reunion/comores-10-cas-confirmes-six-patients-gueris-et-63-cas-contacts-identifies-1668309.html
-
Variole B (mpox) : identification d’un premier cas à La Réunion. Agence Régionale de Santé de La Réunion. 2026. Available from: https://www.lareunion.ars.sante.fr/variole-b-mpox-identification-dun-premier-cas-la-reunion
-
Circulation de la variole B dans l’Océan Indien. MISP n°2026-01. Direction Générale de la Santé. Ministère de la Santé, de la Famille, de l’Autonomie et des Personnes handicapées [Internet]. 2026. Available from: https://sante.gouv.fr/professionnels/article/dgs-urgent
-
Infection au Mpox virus : procédure opérationnelle de prélèvement. Fiche pratique COREB. 2024. Available from: https://www.coreb.infectiologie.com/fr/fiches-pratiques.html
-
Fiche : Gestion des prélèvements biologiques d’un patient suspect ou confirmé d’infection par le virus monkeypox (MPV). Version 4. Société Française de Microbiologie. 2024. Available from: https://www.sfm-microbiologie.org/actualites/monkeypox/monkeypox-fiches/
-
Arrêté du 26 avril 2023 fixant la liste des micro-organismes et toxines prévue à l’article L. 5139-1 du code de la santé publique. JORF n°0123 du 28 mai 2023. Available from: https://www.legifrance.gouv.fr/jorf/id/JORFTEXT000047597611
-
Schuele L, Masirika LM, Udahemuka JC, Siangoli FB, Mbiribindi JB, Ndishimye P, et al. Real-time PCR assay to detect the novel Clade Ib monkeypox virus, September 2023 to May 2024. Euro Surveill. 2024;29(32):2400486.
-
Liste des maladies à déclaration obligatoire. Santé Publique France. Available from: https://www.santepubliquefrance.fr/maladies-a-declaration-obligatoire/liste-des-maladies-a-declaration-obligatoire
-
MONKEYPOX – Aide au diagnostic dermatologique et au traitement symptomatique. Fiche pratiques COREB. 2022. Available from: https://www.coreb.infectiologie.com/fr/fiches-pratiques.html
-
Nouvelles recommandations de traitement des infections sexuellement transmissibles bactériennes. Haute Autorité de Santé. 2025. Available from: https://anrs.fr/actualites/actualites/recommandations-de-prise-en-charge-des-ist/
-
Avis relatif aux mesures de prévention actualisées vis-à-vis de l’infection due au virus monkeypox pour les personnes se rendant dans la zone d’épidémie (voyageurs et professionnels de santé dans le cadre de missions humanitaires). Haut Conseil de Santé Publique. 2024. Available from: Available from: file:///C:/Users/143762/Downloads/hcspa20240902_mesdeprvpoulesvoyvisvisdumpo.pdf
-
Ladhani SN, Dowell AC, Jones S, Hicks B, Rowe C, Begum J, et al. Early evaluation of the safety, reactogenicity, and immune response after a single dose of modified vaccinia Ankara–Bavaria Nordic vaccine against mpox in children: a national outbreak response. Lancet Infect Dis. 2023;23(9):1042–50.
-
Recommandations sanitaires 2025 aux voyageurs. Haut Conseil de Santé Publique. Available from: https://www.hcsp.fr/Explore.cgi/AvisRapportsDomaine?clefr=1439