Place des intégrons dans la dissémination de la résistance aux antibiotiques en clinique et dans l’environnement
Sylvain MEYER, Olivier BARRAUD
UMR INSERM 1092 : Anti-infectieux, supports moléculaires des résistances et innovations thérapeutiques
Faculté de Médecine, Université de Limoges
Service de Bactériologie-Virologie-Hygiène, CHU de Limoges
sylvain.meyer@unilim.fr ; olivier.barraud@unilim.fr
Définition et structure d’un intégron
Les intégrons de résistance ou intégrons mobiles, dénommés par la suite « intégrons », sont des éléments génétiques capables de promouvoir l’acquisition et l’expression de gènes de résistance aux antibiotiques et aux antiseptiques (1). Immobiles par eux-mêmes mais localisés sur des éléments génétiques mobiles tels que les transposons ou les plasmides, ils jouent un rôle clé dans la dissémination de l’antibiorésistance, notamment chez les bactéries à Gram négatif, aussi bien en clinique que dans l’environnement.
Structurellement, la plateforme fonctionnelle d’un intégron est composée de 3 éléments essentiels à savoir :
- Un gène intI qui code pour une intégrase IntI, et dont la séquence en acides aminés permet de déterminer la classe de l’intégron (2). Sont ainsi distingués les intégrons de classe 1, 2 et 3.
- Un site de recombinaison attI reconnu par l’intégrase (3).
- Un promoteur Pc, dont il existe plusieurs variants, localisé dans la séquence codante de l’intégrase et qui assure l’expression des gènes de cassettes intégrées en aval.
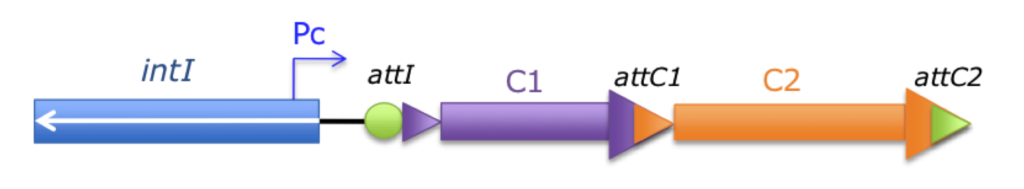
Figure 1 : Structure de base d’un intégron
La plateforme fonctionnelle d’un intégron contient 3 éléments clés : un gène intI qui code une intégrase, un site spécifique de recombinaison attI et un promoteur Pc. Le réseau de cassettes localisé en aval correspond à la partie variable de l’intégron à l’origine de l’expression de l’antibiorésistance. Pc = promoteur de cassettes ; C1, C2 : cassettes hébergeant un gène (généralement un gène de résistance aux antibiotiques) ; attI, attC1, attC2 : sites spécifiques de recombinaison reconnus par l’intégrase ; intI : gène de l’intégrase. (4)
En aval de cette plateforme, l’intégron peut héberger un nombre variable de cassettes (0 à 10), une cassette étant l’association d’un gène (codant notamment des résistances à des antibiotiques) et d’un site attC reconnu par l’intégrase. Les cassettes sont des unités génétiques mobiles qui peuvent facilement être intégrées ou excisées via l’intégrase IntI par un mécanisme de recombinaison spécifique de site grâce à des recombinaisons entre 2 sites attC ou entre le site attI et un site attC. Les cassettes ne possédant pas de promoteur propre, la distance séparant la cassette du promoteur Pc conditionne le niveau d’expression du gène qu’elle renferme. Ce système permet donc le stockage de cassettes éloignées, ayant des gènes peu exprimés, qui pourront être mieux exprimés après recombinaison des cassettes via l’intégrase IntI et rapprochement de celles-ci de Pc, notamment lors d’une exposition aux antibiotiques (5). Les réarrangements liés à l’intégrase peuvent ainsi mener à l’apparition de résistances qui étaient jusque-là portées mais non exprimées.
Les intégrons de classe 1 sont les plus prévalents (mais aussi les plus étudiés) et ils possèdent une grande variabilité de cassettes (6). Les intégrons de classe 2 sont eux plus stables du fait de la présence fréquente d’une intégrase non fonctionnelle (7). Enfin, les intégrons de classe 3 ont été plus rarement décrits mais constituent un réservoir environnemental important (8). Des milliers de cassettes différentes ont été décrites (9) dont des centaines impliquées dans la résistance aux antibiotiques. La résistance aux β-lactamines est fréquemment retrouvée dans les intégrons (pénicillinases, oxacillinases, BLSE voire carbapénémase) tout comme la résistance au triméthoprime, aux aminosides ou au chloramphénicol.
Place des intégrons comme marqueurs de la résistance aux antibiotiques en clinique
Les intégrons sont couramment retrouvés au sein des bacilles à Gram négatif (BGN) isolés chez l’Homme tels que Escherichia coli, Klebsiella spp, Enterobacter spp et autres entérobactérales, Pseudomonas aeruginosa ou encore Acinetobacter baumannii (10). L’augmentation de la résistance de ces BGN est particulièrement préoccupante à l’hôpital et en particulier dans les services de réanimation où les sepsis et pneumopathies acquises sous ventilation mécanique sont fréquentes. Une étude grecque a d’ailleurs démontré qu’un séjour en unité de soins intensifs, une longue durée d’hospitalisation ou l’administration antérieure d’une antibiothérapie par cotrimoxazole, pénicillines +/- inhibiteurs de β-lactamases, aminosides ou quinolones augmentaient le risque de portage d’intégrons (11). Il a été retrouvé qu’environ 10 à 30% des BGN isolés d’hémocultures sont porteurs d’intégrons (12)(13). Comme le montre la Figure 2, la présence des intégrons est corrélée à une multi-résistance chez les entérobactérales (14) et constitue un bon marqueur de l’acquisition de résistance avec une bonne valeur prédictive négative (13). Ceci a été particulièrement mis en évidence pour certains antibiotiques comme les aminosides, le cotrimoxazole, la ciprofloxacine ou les C3G. La recherche d’intégrons directement à partir des prélèvements cliniques par qPCR permettrait ainsi de mieux ajuster l’antibiothérapie probabiliste et de mieux préserver l’utilisation des antibiotiques à large spectre.
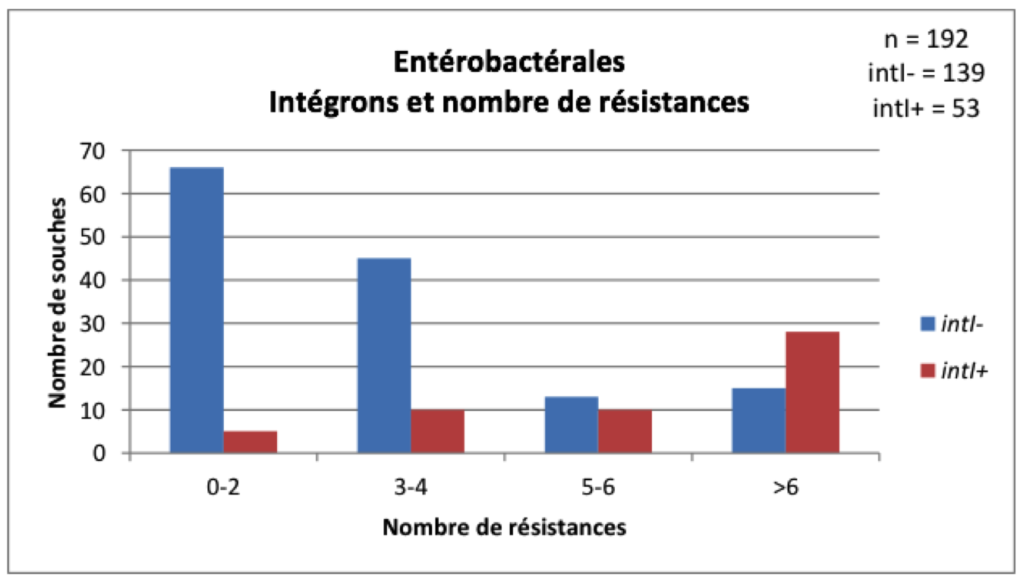
Figure 2 : Lien entre présence d’intégrons et nombre de résistances chez les entérobactérales.
D’après l’étude de Barraud O. et al (13).
intI+ : présence du gène de l’intégrase, intI- : absence du gène de l’intégrase
D’autres entérobactérales comme Proteus, Morganella ou Providencia ont la particularité d’héberger plutôt des intégrons de classe 2 avec un réseau de cassettes relativement stable, pouvant constituer un réservoir (15). Mendes Moreira et al ont montré qu’environ 40% des Proteae isolés en clinique en sont porteurs et que la présence d’intégrons de classe 2 est corrélée à un phénotype de multirésistance, là encore concernant les aminosides, le cotrimoxazole ou les fluoroquinolones.
Chez les bactéries à Gram positif (BGP), les intégrons sont beaucoup plus rarement retrouvés. Quelques publications ont mis en évidence des souches de corynébactéries porteuses d’intégrons de classe 1 (16) comme cela a été décrit chez Corynebacterium diphtheriae avec un intégron impliqué dans la résistance au cotrimoxazole (17). Néanmoins, la prévalence des intégrons chez les BGP étant confidentielle, il n’est pas possible d’utiliser les intégrons chez les BGP comme des marqueurs de résistance.
Place des intégrons comme marqueurs de la résistance aux antibiotiques dans l’environnement
Les eaux usées sont une source majeure de dissémination de la résistance aux antibiotiques dans l’environnement (18). Le biofilm est un milieu particulièrement favorable à l’acquisition et aux échanges de gènes de résistance pour les bactéries (19). Plus de 60% des gènes de résistance retrouvés dans les effluents sont portés par des éléments génétiques mobiles (20) et il est estimé qu’entre 1 et 5% des bactéries retrouvées dans le sol ou l’eau sont porteuses d’intégrons (21). Les usages des antibiotiques dans les fermes d’élevages sont aujourd’hui encore de grands pourvoyeurs de dissémination de l’antibiorésistance dans l’environnement (22). Il est d’ailleurs estimé que 30 à 90% des antibiotiques ingérés sont naturellement excrétés et retrouvés dans les effluents (23), ce qui favorise une plus forte pression de sélection antibiotique environnementale, et donc une plus importante détection des intégrons. En effet, plusieurs études in vitro ont démontré que des concentrations subinhibitrices en antibiotiques pouvaient influencer le comportement bactérien et influencer leurs modifications génétiques (24).
Par ailleurs, il a été démontré que le microbiote digestif est un réservoir important de gènes de résistance aux antibiotiques (25) et que la pollution fécale humaine et animale est corrélée à la dissémination de la résistance par les effluents (26). On peut ainsi distinguer par leur quantité et leur profil en gènes de résistance aux antibiotiques les effluents urbains des effluents hospitaliers. Une étude a ainsi démontré que bien que les effluents hospitaliers ne représentent que 2% du flux des effluents totaux qui arrivent en station d’épuration, ils contribuent à hauteur de 14% de la masse en intégrons de classe 1 détectés (18) (Figure 3). Ils présentent également un profil de résistance différent du reste des effluents, imputable à une plus grande consommation d’antibiotiques à l’hôpital (27)(28). Plusieurs études ont d’ailleurs relevé dans les effluents hospitaliers une plus grande quantité d’entérobactérales porteuses de gènes de résistance dont les BLSE (29)(30).
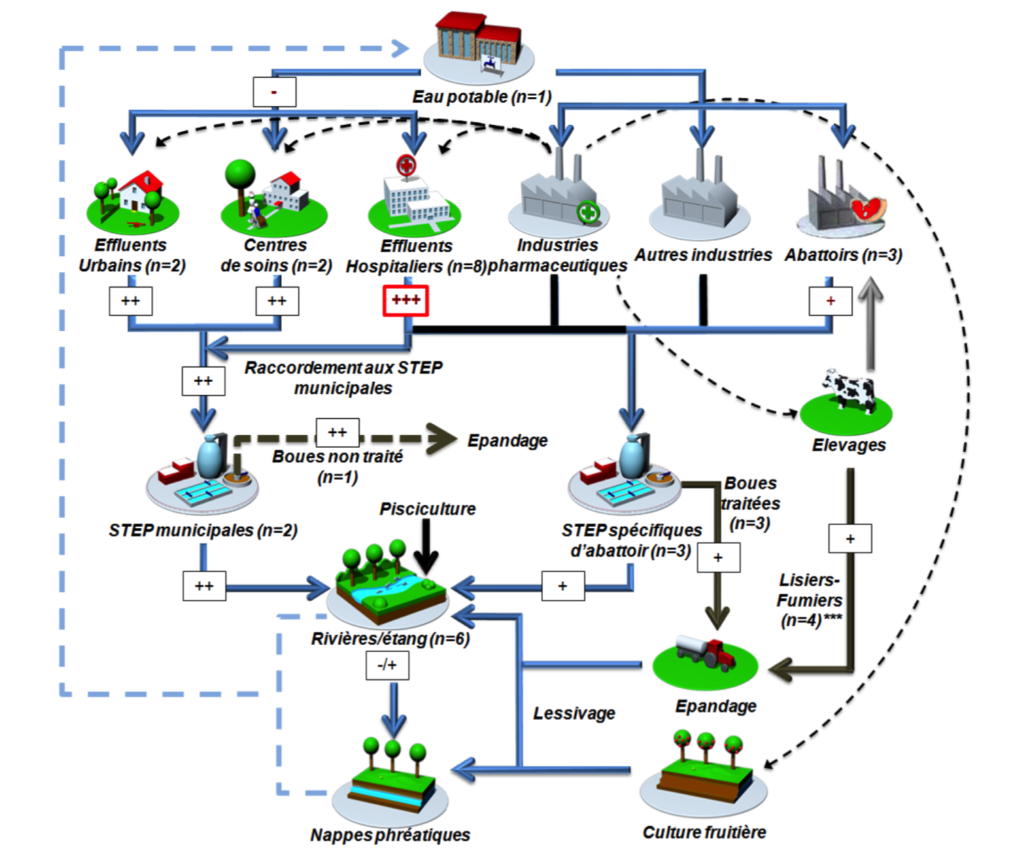
Figure 3 : Principales voies d’entrée des intégrons dans l’environnement, basées sur la proportion d’intégrons dans les communautés bactériennes (abondances relatives).
Les flèches représentent en bleu : les flux d’eau, en marron : les flux de solide, en gris : le cheminement des animaux vers les abattoirs, en pointillées noirs : les consommations d’antibiotiques, et en noir : les effluents non étudiés. Les croix représentent des abondances relatives : + + + ≥ 0,3 et pouvant aller jusqu’à 5 ; 0,3 ≥ + + ≥ 0,03 ; + < 0,1.
Tous ces arguments tendent à démontrer que les intégrons de classe 1 sont considérés aujourd’hui comme des marqueurs de pollution anthropique. Plusieurs études soutiennent ce postulat (31)(32). Ainsi, les intégrons sont particulièrement présents dans l’environnement, ce qui permet aux bactéries hôtes de toujours mieux répondre à la pression de sélection aux antibiotiques, antiseptiques et métaux lourds exercés par l’Homme sur son environnement. Les intégrons sont donc un exemple concret de l’interaction complexe qu’entretiennent les Hommes avec le monde animal et l’environnement en terme d’antibiorésistance (concept OneHealth). (33)(34)
Bibliographie :
- Stokes HW, Hall RM. A novel family of potentially mobile DNA elements encoding site-specific gene-integration functions: integrons. Mol Microbiol. déc 1989;3(12):1669‑83.
- Mazel D. Integrons: agents of bacterial evolution. Nat Rev Microbiol. août 2006;4(8):608‑20.
- Partridge SR, Recchia GD, Scaramuzzi C, Collis CM, Stokes HW, Hall RM. Definition of the attI1 site of class 1 integrons. Microbiol Read Engl. nov 2000;146 ( Pt 11):2855‑64.
- Barraud O, Ploy M-C. Actualités sur les intégrons de résistance aux antibiotiques : mise au point. J Anti-Infect. sept 2011;13(3):133‑44.
- Barraud O, Ploy M-C. Diversity of Class 1 Integron Gene Cassette Rearrangements Selected under Antibiotic Pressure. J Bacteriol. juill 2015;197(13):2171‑8.
- Partridge SR, Tsafnat G, Coiera E, Iredell JR. Gene cassettes and cassette arrays in mobile resistance integrons. FEMS Microbiol Rev. juill 2009;33(4):757‑84.
- Hansson K, Sundström L, Pelletier A, Roy PH. IntI2 Integron Integrase in Tn7. J Bacteriol. 15 mars 2002;184(6):1712‑21.
- Moura A, Henriques I, Smalla K, Correia A. Wastewater bacterial communities bring together broad-host range plasmids, integrons and a wide diversity of uncharacterized gene cassettes. Res Microbiol. févr 2010;161(1):58‑66.
- Moura A, Soares M, Pereira C, Leitão N, Henriques I, Correia A. INTEGRALL: a database and search engine for integrons, integrases and gene cassettes. Bioinforma Oxf Engl. 15 avr 2009;25(8):1096‑8.
- Kaushik M, Kumar S, Kapoor RK, Virdi JS, Gulati P. Integrons in Enterobacteriaceae: diversity, distribution and epidemiology. Int J Antimicrob Agents. févr 2018;51(2):167‑76.
- Daikos GL, Kosmidis C, Tassios PT, Petrikkos G, Vasilakopoulou A, Psychogiou M, et al. Enterobacteriaceae bloodstream infections: presence of integrons, risk factors, and outcome. Antimicrob Agents Chemother. juill 2007;51(7):2366‑72.
- Heir E, Lindstedt B-A, Leegaard TM, Gjernes E, Kapperud G. Prevalence and characterization of integrons in blood culture Enterobacteriaceae and gastrointestinal Escherichia coli in Norway and reporting of a novel class 1 integron-located lincosamide resistance gene. Ann Clin Microbiol Antimicrob. 8 juill 2004;3:12.
- Barraud O, François B, Chainier D, Vignaud J, Ploy M-C. Value of integron detection for predicting antibiotic resistance in patients with Gram-negative septicaemia. Int J Antimicrob Agents. oct 2014;44(4):351‑3.
- Leverstein-van Hall MA, M Blok HE, T Donders AR, Paauw A, Fluit AC, Verhoef J. Multidrug resistance among Enterobacteriaceae is strongly associated with the presence of integrons and is independent of species or isolate origin. J Infect Dis. 15 janv 2003;187(2):251‑9.
- Mendes Moreira A, Couvé-Deacon E, Bousquet P, Chainier D, Jové T, Ploy M-C, et al. Proteae: a reservoir of class 2 integrons? J Antimicrob Chemother. 01 2019;74(6):1560‑2.
- Nandi S, Maurer JJ, Hofacre C, Summers AO. Gram-positive bacteria are a major reservoir of Class 1 antibiotic resistance integrons in poultry litter. Proc Natl Acad Sci U S A. 4 mai 2004;101(18):7118‑22.
- Barraud O, Badell E, Denis F, Guiso N, Ploy M-C. Antimicrobial drug resistance in Corynebacterium diphtheriae mitis. Emerg Infect Dis. nov 2011;17(11):2078‑80.
- Stalder T, Barraud O, Jové T, Casellas M, Gaschet M, Dagot C, et al. Quantitative and qualitative impact of hospital effluent on dissemination of the integron pool. ISME J. avr 2014;8(4):768‑77.
- Strugeon E, Tilloy V, Ploy M-C, Da Re S. The Stringent Response Promotes Antibiotic Resistance Dissemination by Regulating Integron Integrase Expression in Biofilms. mBio. 16 2016;7(4).
- Buelow E, Rico A, Gaschet M, Lourenço J, Kennedy SP, Wiest L, et al. Hospital discharges in urban sanitation systems: Long-term monitoring of wastewater resistome and microbiota in relationship to their eco-exposome. Water Res X. 1 mai 2020;7:100045.
- Gillings MR. Integrons: Past, Present, and Future. Microbiol Mol Biol Rev MMBR. juin 2014;78(2):257‑77.
- Barlow RS, Fegan N, Gobius KS. Integron-containing bacteria in faeces of cattle from different production systems at slaughter. J Appl Microbiol. août 2009;107(2):540‑5.
- Sarmah AK, Meyer MT, Boxall ABA. A global perspective on the use, sales, exposure pathways, occurrence, fate and effects of veterinary antibiotics (VAs) in the environment. Chemosphere. oct 2006;65(5):725‑59.
- Rodríguez-Rojas A, Rodríguez-Beltrán J, Couce A, Blázquez J. Antibiotics and antibiotic resistance: a bitter fight against evolution. Int J Med Microbiol IJMM. août 2013;303(6‑7):293‑7.
- Sommer MOA, Church GM, Dantas G. The human microbiome harbors a diverse reservoir of antibiotic resistance genes. Virulence. août 2010;1(4):299‑303.
- Karkman A, Pärnänen K, Larsson DGJ. Fecal pollution can explain antibiotic resistance gene abundances in anthropogenically impacted environments. Nat Commun. 08 2019;10(1):80.
- Buelow E, Bayjanov JR, Majoor E, Willems RJ, Bonten MJ, Schmitt H, et al. Limited influence of hospital wastewater on the microbiome and resistome of wastewater in a community sewerage system. FEMS Microbiol Ecol. 01 2018;94(7).
- Wang Q, Wang P, Yang Q. Occurrence and diversity of antibiotic resistance in untreated hospital wastewater. Sci Total Environ. 15 avr 2018;621:990‑9.
- Chagas TPG, Alves RM, Vallim DC, Seki LM, Campos LC, Asensi MD. Diversity of genotypes in CTX-M-producing Klebsiella pneumoniae isolated in different hospitals in Brazil. Braz J Infect Dis Off Publ Braz Soc Infect Dis. oct 2011;15(5):420‑5.
- Korzeniewska E, Korzeniewska A, Harnisz M. Antibiotic resistant Escherichia coli in hospital and municipal sewage and their emission to the environment. Ecotoxicol Environ Saf. mai 2013;91:96‑102.
- Gillings MR, Gaze WH, Pruden A, Smalla K, Tiedje JM, Zhu Y-G. Using the class 1 integron-integrase gene as a proxy for anthropogenic pollution. ISME J. juin 2015;9(6):1269‑79.
- Amos GCA, Gozzard E, Carter CE, Mead A, Bowes MJ, Hawkey PM, et al. Validated predictive modelling of the environmental resistome. ISME J. juin 2015;9(6):1467‑76.
- Sikkema R, Koopmans M. One Health training and research activities in Western Europe. Infect Ecol Epidemiol. 2016;6:33703.
- Chainier D, Barraud O, Masson G, Couve-Deacon E, François B, Couquet C-Y, et al. Integron Digestive Carriage in Human and Cattle: A « One Health » Cultivation-Independent Approach. Front Microbiol. 2017;8:1891.